INTRODUÇÃO
A síndrome da
veia cava superior (SVCS) resulta de qualquer condição que leve à obstrução do
fluxo sanguíneo através da veia cava superior (VCS). A obstrução maligna pode
ser causada por invasão direta do tumor na VCS ou por compressão externa da VCS
por um processo patológico adjacente envolvendo o pulmão direito, linfonodos e
outras estruturas mediastinais, levando à estagnação do fluxo e trombose. Em
alguns casos, tanto a compressão externa quanto a trombose coexistem. Além
disso, os pacientes com malignidade têm um risco maior de trombose venosa
quando utilizam dispositivos venosos de demora (por exemplo, cateter venoso
central, marca-passo).
Embora a
invasão direta ou compressão externa do tumor já tenha sido responsável pela
maioria dos casos de síndrome SVCS em pacientes com câncer, a incidência geral
dessa relacionada a dispositivos intravasculares aumentou, agora representando
20 a 40% dos casos.
Esta revisão
se concentrará na fisiopatologia, etiologia, apresentação clínica e avaliação
diagnóstica da síndrome VCS em pacientes com malignidade e no seu tratamento.
FISIOPATOLOGIA
Obstrução da
veia cava superior (VCS) é uma oclusão venosa central torácica tipo IV,
relacionada aos resultados de malignidade da compressão extrínseca da SVCS pelo
tumor primário ou linfonodos mediastinais aumentados, ou como resultado da
invasão direta do tumor na veia cava superior. Pacientes com malignidade também
têm um risco maior de trombose venosa relacionada a dispositivos venosos de
demora (por exemplo, cateter venoso central, marca-passo).
À medida que o
fluxo de sangue dentro da VCS fica obstruído, as colaterais venosas formam vias
alternativas para o retorno do sangue venoso ao átrio direito . As veias
colaterais podem surgir dos sistemas ázigos, mamária interna, torácica lateral,
paraespinhosa e venosa esofágica. As colaterais venosas se dilatam ao longo de
várias semanas. Como resultado, a pressão venosa da parte superior do corpo é
acentuadamente elevada inicialmente, mas diminui com o tempo. No entanto, mesmo
quando padrões de drenagem colateral bem desenvolvidos estão presentes, as
pressões venosas centrais permanecem elevadas, produzindo os sinais e sintomas
característicos da síndrome da VCS.
Pacientes com
doença maligna podem desenvolver sintomas de SVCS rapidamente porque o
crescimento rápido do tumor não permite o tempo adequado para desenvolver fluxo
colateral. Por outro lado, a mediastinite fibrosante devido a uma infecção,
como a histoplasmose, como causa da oclusão da VCS pode não se tornar
sintomática por anos.
O débito
cardíaco pode ser diminuído transitoriamente pela obstrução aguda da VCS, mas
dentro de algumas horas, o retorno do sangue é restabelecido pelo aumento da
pressão venosa e colaterais. O comprometimento hemodinâmico, se presente,
resulta mais frequentemente do efeito de massa no coração do que da compressão
da VCS.
MALIGNIDADES TÍPICAS
Uma
malignidade intratorácica é responsável por 60 a 85% dos casos de SVCS, e a
obstrução da VCS é o sintoma de apresentação de um tumor não diagnosticado
previamente em até 60% desses casos. O câncer de pulmão de células não pequenas
(NSCLC) é a causa maligna mais comum da síndrome de VCS, sendo responsável por
aproximadamente 50% de todos os casos, seguido por câncer de pulmão de células
pequenas (SCLC; aproximadamente 25 a 35% de todos os casos) e linfoma não
Hodgkin (LNH; 10 a 15% dos casos). Juntos, estima-se que o câncer de pulmão e o
NHL são responsáveis por aproximadamente 95% dos casos de SVCS que são causados
por malignidade.
Câncer de
pulmão - Aproximadamente dois a quatro por cento dos pacientes com câncer de
pulmão desenvolvem a SVCS em algum ponto durante o curso da doença. A SVCS é
mais comum com CPCP, ocorrendo em aproximadamente 10% dos casos na
apresentação. Presumivelmente, isso ocorre porque o CPCP se desenvolve e cresce
rapidamente nas vias aéreas centrais, em vez de nas periféricas. Menos de dois
por cento dos pacientes que apresentam NSCLC têm a SVCS como complicação, mas
devido à maior incidência, NSCLC é uma causa mais frequente de SVCS do que o
SCLC.
Linfoma - SVCS
se desenvolve em dois a quatro por cento dos casos de LNH. Por razões pouco
claras, o linfoma de Hodgkin raramente é uma causa da síndrome de VCS, apesar
de sua apresentação comum com linfadenopatia mediastinal.
Outros -
Outros tumores malignos que são menos comumente associados à SVCS incluem
timoma e outras neoplasias tímicas, neoplasias de células germinativas
mediastinais primárias, mesotelioma e tumores sólidos com metástases em
linfonodos mediastinais (por exemplo, câncer de mama ).
MANIFESTAÇÕES CLÍNICAS
A síndrome da
veia cava superior (SVCS) é o sintoma de apresentação de um tumor não
diagnosticado previamente em até 60% dos casos. Portanto, a história deve
incluir a avaliação de fatores de risco conhecidos para os tipos de
malignidades conhecidas por causar a SVCS (por exemplo, tabagismo, exposição ao
amianto).
Sintomas e
sinais - os sintomas e sinais de obstrução venosa central torácica podem
incluir inchaço, dor no peito, sintomas respiratórios ou manifestações
neurológicas. Independentemente da etiologia, edema da face ou pescoço e
dispneia são sintomas de apresentação comuns.
Os pacientes
frequentemente se queixam de edema facial ou plenitude na cabeça, que pode ser
exacerbada pela inclinação para a frente ou deitada, ou edema no braço. O
inchaço da cabeça e do pescoço é visualmente notável, mas geralmente de pouca
consequência clínica. No entanto, o edema pode estreitar a luz das vias nasais
e laringe, podendo comprometer a função laríngea ou faríngea e causar dispneia,
estridor, tosse, rouquidão e disfagia. A dificuldade respiratória também pode
estar relacionada a derrame pleural ou restrição pulmonar decorrente de edema
torácico ou mamário grave.
Além disso, os
pacientes com edema cerebral podem ter dores de cabeça, confusão ou distúrbios
visuais / auditivos. O edema cerebral pode causar herniação do tronco cerebral
e, possivelmente, morte.
A rapidez do
início dos sintomas depende do curso de tempo da invasão ou compressão da VCS e
da gravidade do comprometimento luminal. A presença e gravidade dos sintomas e
sinais de obstrução da VCS, por sua vez, dependem se o recrutamento de
colaterais venosos compensou o estreitamento. A trombose aguda de uma obstrução
parcial estável anterior também pode ocorrer, levando a sintomas abruptos.
Ao exame
físico, pode ser aparente distensão das veias do pescoço e da parede torácica.
Edema do braço, cianose e pletora facial são menos frequentes.
Classificação
da gravidade dos sintomas - Foi proposto um sistema de classificação que
estratifica os sintomas com base na gravidade e também informa a abordagem para
diagnóstico e tratamento. Embora outros sistemas de classificação estejam em
uso, em geral, preferimos esse sistema de classificação, pois informa o caminho
diagnóstico e terapêutico.
Um sistema de classificação separado, mas semelhante, do National Cancer Institute (os Critérios de Terminologia Comum para Eventos Adversos [CTCAE]) classifica a SVCS como um evento adverso durante a terapia do câncer . Os sistemas de graduação são semelhantes, mas os pacientes assintomáticos são considerados de Grau 1 (em vez de grau 0) e os pacientes com sintomas leves ou moderados são agrupados como Grau 2 (em vez de grau 1 ou 2).
INVESTIGAÇÃO DIAGNÓSTICA
Haja vista que
se trata de uma emergência, o diagnóstico ocorre de forma concomitante à
sintomatologia, dessa forma, investigamos as possibilidades de causa desses
sintomas para chegar a conclusão de ser ou não um quadro de SVCS.
Mas quais são
os métodos que utilizamos para descobrir isso? Naturalmente sabemos que
síndromes são sinais e sintomas característicos, mas há necessidade de
comprovação dessa hipótese diagnóstica, tanto de forma laboratorial como por imagem.
LABORATORIAL
De
início, trabalhos sempre com o Hemograma e o Coagulograma, que são exames
gerais, por vezes com resultados rápidos e que vão nos sinalizar o quadro geral
do paciente, além de serem interessantes para diagnosticar a causa oncológica,
caso seja, por exemplo, um linfoma leucimizante.
Algo que pode
gerar certa confusão é o fato de as condutas para SVCS serem dirigidas de forma
a diagnosticar a causa (via de regra, oncológica), uma vez que se subentende
que essa síndrome se manifesta em casos mais avançados e que normalmente estão
em tratamento. A lógica está no fato de não se poder afirmar que o paciente
refratário do tumor está em uma unidade a qual seu quadro é conhecido ou que
haja acompanhante para informar em tempo hábil as nuances do caso, por isso é
adotada essa postura de cautela.
Quando há
opção de testar a função renal, o exame laboratorial possibilita a utilização
de uma importante via de imagem, que são exames de contraste. Há essa
necessidade de teste da função renal porque há uma possibilidade razoável de
que ocorra Nefropatia Induzida por Contraste (NIC).
IMAGEM
Conhecida
a polêmica sobre os exames de contraste, podemos partir para a imagiologia
menos arriscada e que é mais sensível no que toca a identificação da neoplasia,
mesmo específica nesse aspecto. Aqui se destaca a radiografia do tórax, que
constata alteração em 85% dos casos de SVCS, sendo essas alterações:
Cerca de 25% das vezes sendo um
Derrame Pleural
E aproximadamente 64% sendo um
alargamento do mediastino
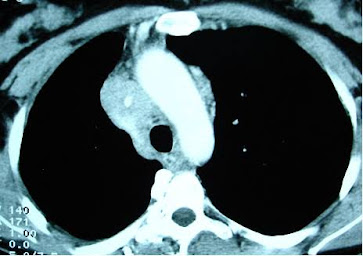
Por motivo de velocidade e até disponibilidade, o raio-x é o mais utilizado e normalmente já nos dirige a um diagnóstico, contudo, uma tomografia computadorizada nos produz uma imagem de grande qualidade, permitindo, assim, entender melhor as compressões que a VCS pode sofrer, como podemos ver na imagem 4:
As setas amarelas apontam para os tumores obstrutores e a seta vermelha para a veia cava superior.
Supondo então que é chegado o paciente com o esses exames e estabelece-se o diagnóstico para Síndrome da Veia Cava Superior, no entanto, antes de tratar desse paciente, devemos definir o grau que a síndrome se encontra.
GRADAÇÃO E CONDUTAS DE EMERGÊNCIA
As
literaturas atuais definem a evolução da doença via gradação de 0 a 5,
dividindo seus sinais e sintomas entre eles para definir do menos grave (grau
zero) ao mais grave (grau cinco):
Grau 0 –
Assintomático, 10% dos casos
Grau 1 – Edema,
cianose e pletora, 25% dos casos
Grau 2- Impacto
funcional leve, 50% dos casos
Grau 3 – Início
dos sintomas graves, 10% dos casos
Grau 4-
Estridor, síncope e hipotensão, 5% dos casos
Grau 5 – Morte, 1% dos casos
É possível perceber que
há um pequeno abismo de gravidade entre os graus, especialmente entre o 2 e o
3, assim, as condutas que o emergencista irá adotar são diferentes.
CONDUTA DE GRAU 0 A 2
Aqui estamos lidando com um paciente de
características menos letais, dessa forma, nossa abordagem pode ser dividida em
três partes, considerando-se que não há conhecimento prévio sobre o paciente e
seu possível cancro:
1- TC Venosa com contraste ou RM se há alergia ao contraste
2- Biópsia da massa obstrutora
3-
Identificação da natureza do
tecido e tratamento específico.
CONDUTA DE GRAU 3 E 4
Já
quando se vê pacientes nessa situação, teremos uma emergência de fato, nesses
casos a conduta é mais complexa e detalhada, podendo ser dividida em 5 partes:
1-
Estabilização – Basicamente
evitar que o paciente curse com um quadro letal, recomenda-se o uso do ABCDE
para que possa ser dirigida intubação e medicação, caso necessário.
2-
Venografia venosa com
intervenção – Aplicação de tratamento prévio com stent, que será discutido mais
a frente nesse artigo.
3- TC Venosa com contraste ou RM se há alergia ao contraste
4- Biópsia da massa obstrutora
5-
Identificação da natureza do
tecido e tratamento específico.
Algo que deve
ser lembrado com veemência é o cuidado que deve ser tomado para não atrapalhar
o prognóstico do paciente por inviabilização da identificação do tipo
histológico na biópsia durante as condutas, por exemplo, a aplicação de corticóide (muito utilizado na estabilização
do paciente) impede identificação de alguns linfomas, assim como uma
radioterapia precoce inviabiliza identificação por biópsia.
TRATAMENTO
Chegando a essa última fase
comum das condutas para SVCS de qualquer grau, é mister entender que sua
precisão depende da história clínica do paciente, dos exames realizados e da
análise histológica, sendo essa última a mais importante por tipificar o tumor.
As opções terapêuticas são 4 (quatro): tratamento clínico, tratamento
radioterápico, tratamento quimioterápico, tratamento endovascular e tratamento
cirúrgico.
TRATAMENTO
CLÍNICO
Oferecido inicialmente para
diminuir sintomas antes de se conseguir conduta específica, sendo então um
conjunto de medidas simples, como repouso, elevação da cabeça e
oxigenioterapia, que produzem conforto leve imediato.
Mas há também o uso empírico
de medicamentos, que não possuem comprovação científica que deem suporte ao seu
uso, como é o caso dos corticoesteróides diuréticos, que tendem a elevar o
risco de trombose por desidratação e podem dificultar a identificação
histológica na biópsia.
TRATAMENTO
RADIOTERÁPICO
Método
mais utilizado para tratar SVCS, posto que 90% dos
casos decorrem de neoplasia , pode ser exclusiva ou adjuvante à quimioterapia e possui
eficácia contra maior parte das neoplasias causadoras, especialmente as
pulmonares.
Tende a produzir sinais clínicos animadores
TRATAMENTO QUIMIOTERAPIA
Muito
similar ao tratamento radioterápico no que diz respeito a respostas, ele possui
uma boa taxa de melhora, principalmente em tumores sensíveis a sua ação, como
linfomas e tumores germinativos. Vale salientar que ao longo prazo, produz uma
melhora de até 80% dos sintomas.
TRATAMENTO ENDOVASCULAR
Basicamente se concentra na aplicação de um stent , técnica que vem ganhando força nos últimos anos, principalmente quando olhado sua melhora veloz que possui intervalo de apenas um dia que pode ser feita de forma imediata, visto que seu uso não impede identificação por biópsia.
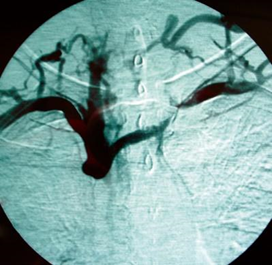
Imagem 5: Hoff, 2013
À esquerda, uma veia cava
superior obstruída e à direita essa veia desobstruída por implantação de stent. Note o claro restabelecimento de fluxo.
Mas é interessante salientar que ele não trata a doença base, mesmo assim, sua efetividade paira dos 80-100%, e com baixa taxa de reobstrução. Todavia, algo que deve ser lembrado é o fato de que, quando realizado, cursa com óbito de 2%, o que pode parecer pouco se o curso natural de SVCS não incidisse em 1% de óbitos.
TRATAMENTO CIRÚRGICO
As intervenções cirúrgicas consistem na aplicação de enxertos venosos, artificiais(Gore-tex/PTFE e Dracon) ou homólogos(comumente veia safena/bypass) e possuem taxa de qualidade elevadíssima, mas é reservado a casos benignos, haja vista questões de expectativa de vida(discutidas em prognóstico). Algo que vem tendendo a mudar, haja vista as melhoras de prognóstico que vem sendo alcançadas com a evolução dos tratamentos.
PROGNÓSTICO
A
SVCS é uma emergência que em 90% das vezes advém de um caso oncológico, assim
sendo pode ser dividida em dois prospectos:
Benigno 🡪 Normalmente expectativa de vida alta, podendo o paciente
por vezes seguir com a vida normalmente.
Maligno 🡪Normalmente expectativa de vida de aproximadamente 6 meses com variações de 1,5 a 9,5 meses.
REFERÊNCIAS
- Drews RE, Rabkin DJ. Malignancy-related
superior vena cava syndrome. In: UpToDate, Post TW (Ed), UpToDate,
Waltham, MA. (Accessed on July 21, 2014).
- Hoff, Paulo Marcelo Gehm (ed). Tratado de
oncologia. SÃO PAULO: ATHENEU, 2013.
- Ingledew P. Oncology emergencies for
medical students, PowerPoint presentation, FVCC, Surrey.
- MARTINS,Herlon Saraiva;
BRANDÃO NETO, Rodrigo Antonio; VELASCO, Irineu Tadeu. Medicina
- de emergência: abordagem prática. In: Medicina de emergência: abordagem
prática. 2016. p. 1509-1509
- Nickloes TA. (2012). Superior vena cava
syndrome. Retrieved July 21, 2014 from
http://emedicine.medscape.com/article/460865-overview
- ROSA,George Ronald
Soncini da et al. Tratamento cirúrgico da síndrome da veia cava superior
causado por timoma invasivo. BrazilianJournal
of Cardiovascular Surgery,v. 25, n. 2, p. 257-260, 2010.
- Síndrome da Veia Cava
Superior. Disponível em: https://www.medicinanet.com.br/conteudos/revisoes/7632/sindrome_da_veia_cava_superior.htm>
Cristiano H Cajado
Estudante de Medicina da FMB-UFBA
Vice-presidente da
LAON
Discípulo de Drauzio
Varella
Marina Machado
Medicina UniFTC - 7º
semestre
Diretoria de Extensão
da LAON







Comentários
Postar um comentário